La chimica è una materia scientifica veramente affascinante. Grazie alla chimica, gli scienziati cercano di comprendere tutto ciò che ci circonda, fino a porre domande su come l’universo si sia formato e come evolverà.
Tutta la materia è costituita da atomi e molecole, ed è proprio attraverso le loro interazioni che si realizzano le trasformazioni e i cambiamenti che sono oggetto principale dello studio della chimica.
Immaginate per un momento di costruire un oggetto qualsiasi con i “lego”. Ecco, i “lego” che costituiscono qualsiasi oggetto nel mondo reale sono gli atomi e le forze che li tengono uniti sono i legami chimici.

Risulta evidente quindi che come ogni lego, anche atomi e molecole hanno forme e strutture diverse nello spazio e le interazioni che li tengono uniti cambiano. Qui entra in gioco la stereochimica. Non è una parolaccia!
Cosa si intende per stereochimica?
La stereochimica è una branca della chimica, che si occupa dello studio della disposizione spaziale degli atomi all’interno di molecole o di aggregati molecolari e della loro influenza sulle proprietà chimiche e fisiche.

La parola stereo- stèreo deriva dal greco “στερεο” e significa “tridimensionale”, quindi la stereochimica aiuta a comprendere come la disposizione degli atomi nello spazio possa determinare il modo in cui una molecola interagisce con altre molecole.
Ma perché per noi è così importante comprendere la forma spaziale delle molecole?
Sebbene le molecole siano entità così minuscole, la loro forma può avere un impatto significativo sul comportamento e sulle interazioni che avvengono nel mondo macroscopico.
Una parte veramente interessante della stereochimica è la stereoisomeria.
Che cos’è la stereoisomeria?
Questo concetto è molto complesso da descrivere in un articolo di divulgazione scientifica, basti pensare che esistono interi esami all’università o ricerche che si basano proprio sulla stereoisomeria. Ma niente paura, cerchiamo di chiarire le idee!
La stereoisomeria è un concetto fondamentale nella stereochimica che si riferisce alla presenza di molecole con la stessa formula chimica, ma con una diversa disposizione spaziale degli atomi. Questa differenza nella struttura tridimensionale può comportare proprietà chimiche completamente diverse. Quindi gli isomeri sono composti chimici diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e la stessa formula che i chimici chiamano “bruta”.
Alla domanda se gli isomeri sono composti diversi pur avendo gli stessi atomi, la risposta è si! Sono composti diversi e hanno proprietà diverse tra loro perché è diverso il modo in cui gli stessi atomi sono tra loro collegati: hanno perciò formule di struttura differenti.
Nella stereoisomeria gli isomeri si dividono in due categorie:
- ISOMERI DI STRUTTURA O COSTITUZIONALI: di catena, di posizione e di funzione;
- STEREOISOMERI: Isomeri configurazionali e conformazionali.
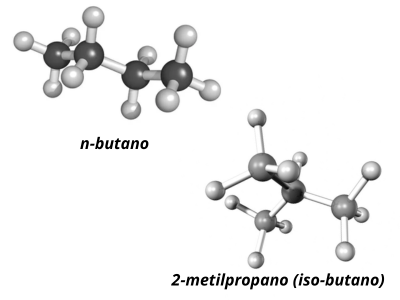
Per farla breve, immaginiamo una semplice molecola organica come il butano, formata da 4 atomi di carbonio e 10 atomi di idrogeno. In chimica organica, il butano ha questa formula bruta C4H10 . Ma di questa formula appena scritta ne esiste un altro di composto, totalmente diverso per caratteristiche chimiche e fisiche, si chiama 2-metilpropano (o isobutano).
Ecco il butano e il 2-metilpropano sono isomeri di struttura, stessa composizione di atomi, ma diversa disposizione di questi nello spazio. Quindi sono due cose totalmente diverse.

Se invece, parliamo di stereoisomeri, sono composti formati da atomi legati nello stesso ordine e sequenza, ma che differiscono, invece, per la loro disposizione spaziale nella molecola. Essi si distinguono in: isomeri configurazionali e isomeri conformazionali.
Ma oggi ci soffermeremo maggiormente sulla stereoisomeria configurazionale e soprattutto sulle molecole dette chirali.
Cosa sono gli isomeri configurazionali?
L’isomeria configurazionale è una forma di isomeria spaziale (stereoisomeria) che si divide in enantiomeria e diastereoisomeria. Sono enantiomeri gli isomeri configurazionali chirali. Gli isomeri configurazionali sono fisicamente separabili ed è possibile che essi si interconvertono solo per rottura e riformazione di legami covalenti.
Si basa sulla presenza di centri stereogenici, come gli atomi di carbonio legati a 4 atomi diversi, che conferiscono alla molecola una diversa configurazione tridimensionale.

Gli enantiomeri sono immagini speculari l’uno dell’altro e non possono sovrapporsi tramite rotazione o traslazione. Questa proprietà di simmetria speculare è associata al concetto di chiralità. Per esempio le mani sono l’una immagine speculare dell’altra, ma non sono sovrapponibili, quindi sono chirali; al contrario una pallina è achirale, poiché è perfettamente sovrapponibile alla sua immagine speculare.
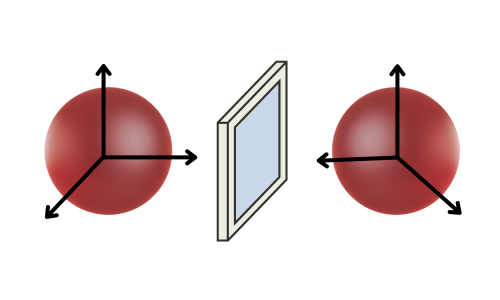
Cosa si intende per chiralità?
Le molecole chirali, quindi, presentano enantiomeri che possono differire nella loro attività biologica, reattività chimica e interazioni con altre molecole. Gli enantiomeri hanno proprietà fisiche identiche (p. ebollizione, p. fusione, solubilità etc), ad eccezione dell’attività ottica e proprietà chimiche identiche, con l’esclusione della interazione con reattivi chirali (otticamente attivi).
La storia della scoperta della chiralità e degli enantiomeri è affascinante e risale al 1848, quando il chimico francese Louis Pasteur fu il primo a dimostrare l’esistenza di molecole chirali.

Pasteur stava studiando il tartrato di sodio, un composto chimico presente nel vino e noto per formare cristalli. Durante i suoi esperimenti, Pasteur notò che i cristalli di tartrato di sodio erano di due tipi differenti, ma molto simili. Sottoponendo i cristalli a una serie di analisi e osservazioni, scoprì che si trattava di enantiomeri, cioè di molecole chirali che erano immagini speculari l’una dell’altra.
Successivamente, nel 1874, il chimico olandese Jacobus van ‘t Hoff e il chimico francese Joseph Achille Le Bel svilupparono la teoria della struttura tridimensionale delle molecole chirali.
La chiralità e la presenza di enantiomeri sono fenomeni ampiamente diffusi nella natura.
Come scrisse lo stesso Pasteur nel 1883 : “tutte le specie viventi, nella loro struttura e nella forma esterna, sono funzione dell’asimmetria del cosmo”.
Non solo la Natura è chirale, ma esiste in gran parte come solo un enantiomero tra i due possibili e in ogni caso sa distinguere il senso di chiralità in forme del regno vegetale e animale.

L’importanza biologica della chiralità.
Molte molecole biologicamente attive, come gli aminoacidi, gli zuccheri e gli acidi nucleici, sono chirali. La chiralità può influenzare la forma e la funzione delle biomolecole e giocare un ruolo essenziale nei processi biologici.
Essa è rilevante nei sistemi biologici e l’attività biologica di un prodotto naturale o l’attività farmacologica di un prodotto di sintesi è spesso correlata con le proprietà stereochimiche.
Facciamo alcuni esempi concreti. Avete mai sentito parlare di un composto chimico chiamato “limonene”? Ovviamente il nome ci suggerisce un’idea!
Il limonene è un composto chimico che contribuisce all’aroma caratteristico degli agrumi, inclusi l’arancio e il limone. Esistono due forme enantiomeriche del limonene, chiamate R-limonene e S-limonene, che sono immagini speculari non sovrapponibili l’una dell’altra. Queste forme enantiomeriche differiscono nella disposizione spaziale degli atomi, anche se hanno la stessa formula chimica. I recettori olfattivi nel naso umano sono sensibili alla configurazione spaziale dei composti chimici, compresi gli enantiomeri. Ciò significa che i recettori olfattivi possono riconoscere e distinguere l’enantiomero R del limonene dall’enantiomero S. Anche se in realtà la situazione è molto diversa.
Sia arance che limoni contengono quasi esclusivamente (R)-limonene:
circa 96–99% (R)-limonene solo 1–4% (S)-limonene
Quindi la differenza di profumo, in questo caso non dipende dal limonene.

Altri esempi noti in natura sono il carvone, estratto dal cumino, presenta odori diversi a seconda dell’enantiomero. Uno da la sensazione di odore di cumino, l’altro di menta.

https://commons.wikimedia.org/wiki/File:Carvone.svg#/media/File:Carvone.svg
E la questione diventa molto più importante se identifichiamo la funzione biologica degli enantiomeri per alcuni farmaci.

Un esempio degno di nota è l’etambutolo, la molecola che è il principio attivo di un farmaco usato contro la tubercolosi. La tubercolosi è una malattia infettiva e contagiosa, causata da un batterio, il Mycobacterium tuberculosis, che nella maggior parte dei casi interessa i polmoni. Se non trattata può portare al decesso. E’ usato come un tubercolostatico attivo sui micobatteri resistenti alla isoniazide ed alla streptomicina ed in ciò consiste il suo particolare valore clinico.
Si prepara per sintesi e solo la forma destrogira è utilizzata in terapia, mentre l’enantiomero levogiro non ha interesse in tal senso, anzi l’altro enantiomero, può essere associato a effetti collaterali significativi, come epatotossicità e neurite ottica.
Per fare un esempio, il farmaco L-dopa, utilizzato nel trattamento del morbo di Parkinson, è l’enantiomero attivo, mentre il suo enantiomero D-dopa è inattivo. In molti casi, è necessario separare gli enantiomeri e utilizzare solo quello attivo per ottenere gli effetti desiderati e ridurre al minimo gli effetti collaterali.

Invece la talidomide è un farmaco che è diventato noto per la sua storia tragica e l’impatto negativo che ha avuto sulla salute di molte persone.
La talidomide è un composto chirale, il che significa che esiste in forma di enantiomeri. Questa molecola veniva commercializzata tra gli anni cinquanta e sessanta e usata come sedativo e anti-nausea soprattutto per le donne in gravidanza. Inizialmente, è stata commercializzata come una miscela racemica di entrambi gli enantiomeri. Era un farmaco molto promettente. Tuttavia, nei primi anni sessanta furono riportati i primi episodi di focomelia, vale a dire ridotta o addirittura mancata formazione degli arti nei bambini. Questo farmaco rappresentò forse l’esempio più drammatico di come due molecole praticamente identiche, ma con diversa disposizione nello spazio, potessero avere effetti diametralmente opposti. Un enantiomero era sicuro, l’altro no.

Però da un evento sicuramente così negativo, tale scoperta ha sottolineato l’importanza della separazione degli enantiomeri nella produzione e nell’uso dei farmaci per evitare effetti indesiderati.
In conclusione, la comprensione della chiralità e della stereochimica riveste un ruolo fondamentale nella scienza. L’importanza biologica della chiralità è evidente anche nella nostra esperienza quotidiana. La sua importanza nel campo della scienza e della medicina continua a crescere, offrendo nuove prospettive e promettenti opportunità per il futuro.
Dott. Francesco Domenico Nucera
FONTI:
- https://piccolocimento.dcci.unipi.it/archivio/numero-2/lezioni-stereochimica-talidomide.html
- Eliel, E.L., Wilen, S.H., Doyle, M.P. 2001, Basic Organic Stereochemistry, New York, Wiley Interscience
- Primo Levi – L’asimmetria e la vita
- Welch, C.J. 2002, Chirality in the natural world: life through the looking glass, In W.J. Lough and I.W. Wainer, Chirality in natural and applied science (pp.285-302), Oxford, Blackwell Science
- “Chirality in Drug Design and Synthesis” di Indra K. Reddy
- “Organic Chemistry” di Jonathan Clayden, Nick Greeves, Stuart Warren e Peter Wothers
- https://pilloledichimica.it/2021/10/12/the-nobel-prize-in-chemistry-2021/

